L’idée qu’un instrument non stérile soit utilisé lors d’une procédure médicale suffit à donner des frissons à tout patient. Une simple recherche sur Google montre que les équipements chirurgicaux et de diagnostic sales, tels que les endoscopes, restent omniprésents dans les soins de santé et peuvent constituer une menace pour la sécurité des patients en augmentant potentiellement le risque d’infections du site opératoire (ISO).
S’il est essentiel d’atténuer tout risque de déviation des processus de stérilisation au sein d’un établissement de santé, il est également important de prêter attention à la manière dont les instruments stérilisés sont stockés et transportés par la suite. Les systèmes d’emballage stérile jouent un rôle essentiel en garantissant la stérilité des instruments jusqu’à leur prochaine intervention chirurgicale, mais ils sont souvent négligés.
Aujourd’hui, il existe plusieurs systèmes d’emballage stérile pouvant être utilisés dans le service de stérilisation centrale (SC), notamment des conteneurs rigides, des sachets pelables en plastique et/ou en papier, et des enveloppes de stérilisation (constituées de matériaux tissés ou non tissés). Chaque option comporte ses propres risques potentiels pour la sécurité des patients. Heureusement, des données sont disponibles pour aider les organismes de santé à identifier ces zones de risque cachées au sein de leur propre département CS et à mettre en place des stratégies pour réduire ces risques.
Analyse de la littérature
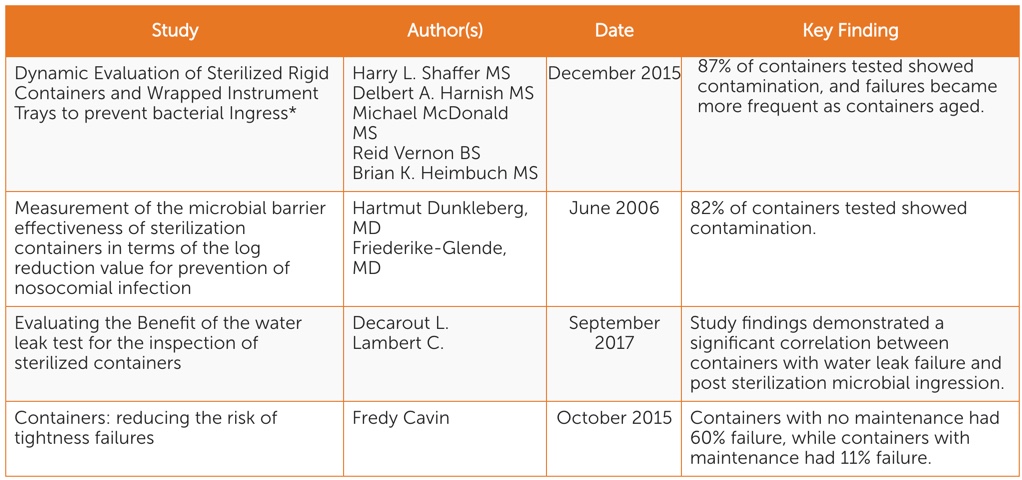
Au cours des 13 dernières années, quatre études scientifiques évaluées par des pairs ont été menées sur l’identification et l’atténuation des risques liés aux systèmes d’emballage stérile (voir tableau 1). Si chacun d’entre eux se concentre sur des aspects différents du maintien de la stérilité, tous mettent l’accent sur les considérations clés suivantes :
- Lorsque des conteneurs rigides sont utilisés, il existe un risque de contamination des instruments pendant le stockage et le transport.
- Les conteneurs rigides deviennent moins efficaces pour maintenir la stérilité des instruments avec le temps.
- L’inspection visuelle ne suffit pas à identifier les risques de stérilité des systèmes d’emballage stérile. Le test à l’eau est un test de fonctionnalité standardisé simple et efficace qui peut être utilisé en conjonction avec une inspection visuelle.
Article connexe
Considérer la conformité
Les problèmes potentiels de performance inhérents à certains types de systèmes d’emballage stérile ne sont pas le seul facteur à prendre en compte en matière de conformité. L’utilisation d’un mélange de systèmes d’emballage stérile – ce qui est courant – ou la pression exercée pour répondre à la demande de débit peuvent également avoir un impact sur le respect des instructions d’utilisation (IFU) du fabricant d’un système d’emballage stérile. Tout ce qui n’est pas conforme à 100 % aux IFU peut entraîner un traitement inadéquat et avoir un impact sur les performances de l’emballage de stérilisation. En livrant au bloc opératoire des instruments chirurgicaux qui n’ont pas été contrôlés ou traités correctement, les services CS peuvent donner un faux sentiment de confiance à ceux qui les utiliseront et mettre potentiellement les patients en danger.
De la connaissance à l'action
Il est impossible d’éliminer tout risque lié au traitement stérile et au système d’emballage stérile utilisé en cours de route, mais il existe un certain nombre de moyens permettant aux organisations de soins de santé de réduire les menaces potentielles pour la sécurité des patients :
- Formation continue : La composition de votre système de conditionnement stérile peut changer d’une année à l’autre, et avec elle les IFU correspondantes. Développez un programme qui évalue et renforce les compétences des utilisateurs pour tous les systèmes de conditionnement stérile utilisés dans votre service CS.
- Évaluation approfondie : Effectuez une évaluation des risques des systèmes d’emballage stérile au moins une fois par an et à chaque changement d’équipement ou de processus. Une évaluation approfondie des risques doit prendre en compte l’âge moyen du stock de conteneurs, le respect des IFU, l’intégrité et la réparation du système d’emballage stérile et les taux de déchirure.
- Collaboration réussie : Une fois que vous avez les données et les considérations spécifiques à votre propre organisation, partagez ces informations à grande échelle pour assurer la collaboration sur l’atténuation des risques avec les partenaires clés du département CS, y compris la chirurgie et la prévention des infections.
La protection de la sécurité des patients est une responsabilité partagée par toutes les organisations de soins de santé. Bien que les ISO soient en baisse, il est essentiel que les professionnels de la santé continuent à identifier les nouvelles sources potentielles d’infection, y compris les systèmes de conditionnement stérile, et à travailler en collaboration pour atténuer ces risques.
* La recherche a été financée par Halyard et menée par Applied Research Associates, un laboratoire de recherche international. Halyard n’a pas eu d’implication directe dans l’exécution de l’étude. L’étude a eu lieu dans un laboratoire indépendant à Panama City, FL, et l’étude a été menée par des chercheurs indépendants.
